Strukturní podstata regulace ubiquitin ligásy Nedd4-2 prostřednictvím proteinů 14-3-3
- Naše výsledky poskytují strukturní pohled na regulaci lidské ubiquitin ligásy Nedd4-2 prostřednictvím proteinů 14-3-3. Naše data by mohla být důležitá k porozumění procesu regulace Nedd4-2 stejně tak jako úloze proteinů 14-3-3 v regulaci ostatních ubiquitin ligáz.
Náš výzkumný tým se zabývá studiem 14-3-3 proteinů, což jsou konzervované regulační molekuly exprimované ve všech eukaryotických buňkách. Poprvé byly izolovány z hovězího mozku a jejich zajímavé jméno „14-3-3“ se odvíjí od jejich migrace na DEAE celulosové chromatografii a škrobové gelové elektroforéze. 14-3-3 proteiny mají schopnost se vázat na funkčně rozdílné signální proteiny, včetně kinas, fosfatas a transmembránových receptorů a tím pozměňovat jejich funkci. Tyto proteiny se účastní signální transdukce, kontroly buněčného cyklu, kontroly metabolismu a apoptosy díky strukturním a funkčním změnám řady svých vazebných partnerů.
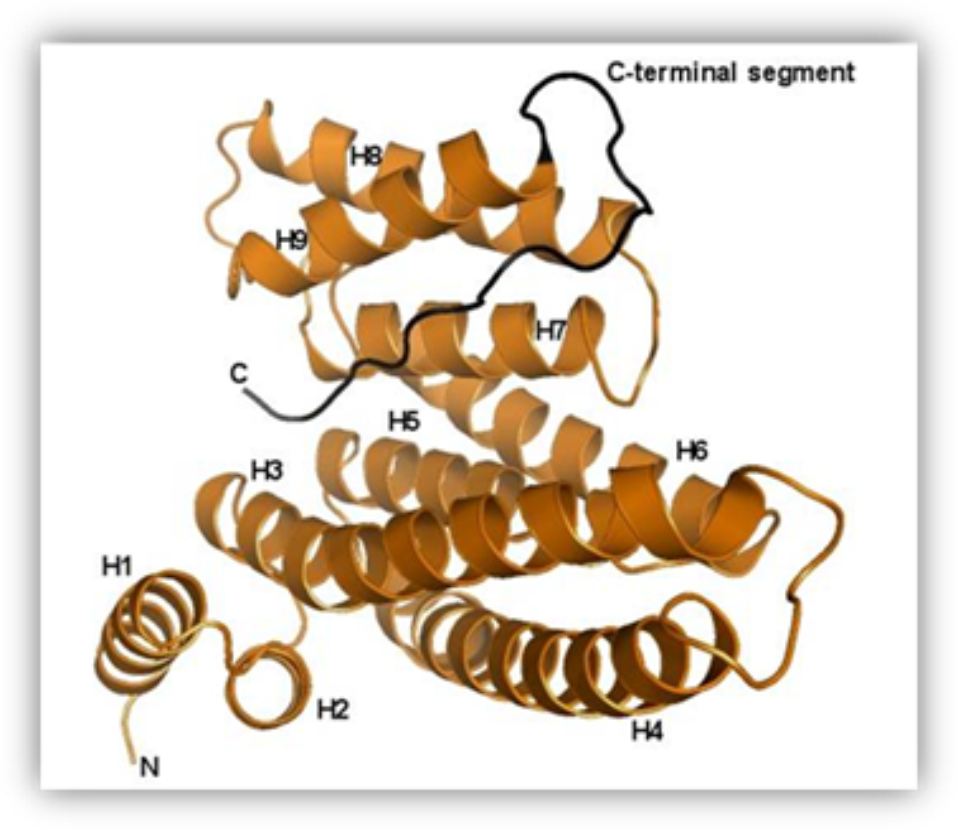
Struktura lidského 14-3-3 proteinu (isoforma zeta) s namodelovaným C-koncovým segmentem.
Odhalení mechanismu inhibice lidské ubiquitin ligázy Nedd4-2 prostřednictvím proteinu 14-3-3
Neurální prekurzor exprimovaný jako vývojově redukovaná buňka 4 (Nedd4-2) je členem rodiny HECT E3 ubikvitin ligáz. Tento enzym se zaměřuje na proteiny určené k ubikvitinaci při programované buněčné smrti savců. Nedd4-2 má modulární multidoménovou architekturu, která se skládá z N-koncové domény C2, čtyř domén WW, které obsahují dva konzervované tryptofanové zbytky a prolinový zbytek, a C-koncové katalytické domény HECT. Nedd4-2 je také regulován fosforylací na třech místech (Ser342, Thr367 a Ser448) rozpoznávaných proteinem 14-3-3. Strukturní analýza založená na SAXS v kombinaci s chemickým síťováním a fluorescenční spektroskopií poskytla první vhled do inhibice Nedd4-2 zprostředkované 14-3-3 a ukázala, že vazba 14-3-3 vyvolává strukturní změnu Nedd4-2 změnou interakcí mezi jeho strukturovanými doménami (Pohl et. al 2021). Kromě toho vznik komplexu způsobuje jak sterickou překážku domén WW3 a WW4, tak konformační změnu katalytické domény HECT (Joshi et al., 2022). Protože domény WW pravděpodobně zprostředkovávají vazbu Nedd4-2 na jeho substráty, takové okluze v kombinaci s konformačními změnami v katalytické doméně pravděpodobně ovlivňují ubikvitinaci substrátů, čímž se vysvětlují modulaci ubikvitinace některých substrátů Nedd4-2 zprostředkovanou 14-3-3.
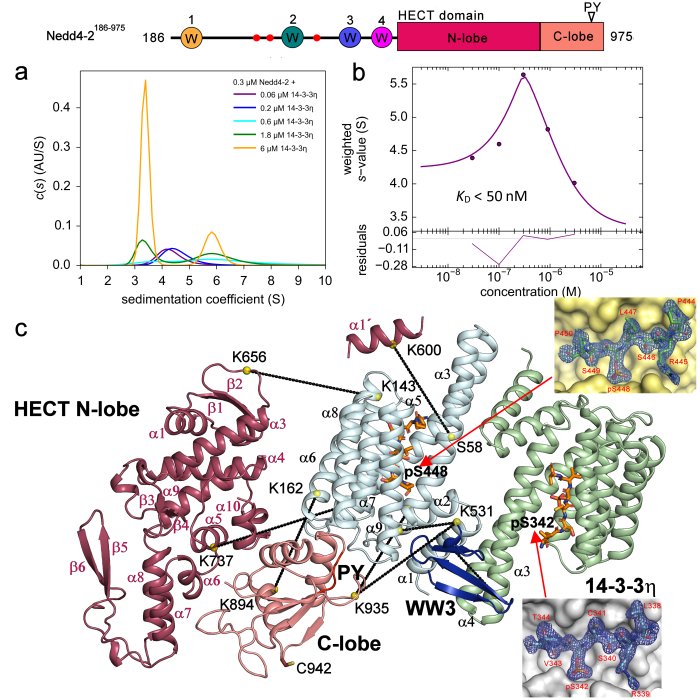
Strukturní analýza komplexu mezi Nedd4-2 a proteinem 14-3-3 pomocí integrativního přístupu strukturní biologie. a)+b) Měření sedimentační rychlosti analytické ultracentrifugace (SV-AUC) s odhadem zdánlivé disociační konstanty komplexu. c) Strukturní modelování na základě SAXS s krystalovými strukturami vazebných míst 14-3-3 Nedd4-2 (Pohl et. al (2021) Communications Biology).
14-3-3 proteiny a ubiquitin ligáza Nedd4-2
V roce 2021 jsme pomocí série biochemických a biofyzikálních metod objasnili, že klíčová místa pro interakci s proteinem 14-3-3 jsou místa pSer342 a pSer448, objasnili jsme princip této interakce vyřešením krystalové struktury 7NMZ a zjistil jsme, že vazba 14-3-3 proteinu blokuje WW3 v centrálním kanálu proteinu 14-3-3 (Pohl et. al 2021).
V roce 2022 jsme pomocí metod fluorescenční spektroskopie objasnili, že 14-3-3 protein snižuje mobilitu a zároveň přístupnost k rozpouštědlu u WW2, WW3 a WW4 domén Nedd4-2. Naopak vazba protienu 14-3-3 má opačný vliv na aktivní místo HECT domény, které je více exponované k rozpouštědlu a více mobilní v komplexu 14-3-3:Nedd4-2 (Joshi et al., 2022).
Současné projekty zahrnují:
1. Úloha vápenatých iontů v regulaci Nedd4-2 a změny struktury vyvolané vazbou vápníku
2. CryoEM komplexu 14-3-3:Nedd4-2
3. Hledání nových E3 ubikvitin ligáz regulovaných proteiny 14-3-3
