Transportéry patogenních kvasinek a lipidy jejich membrán jako cíl nových léčiv
Studujeme vliv lipidového složení plazmatické membrány na citlivost kvasinek k antimykotikům (Kodedová a Sychrová, 2015; Kodedová a kol., 2019; Csáky a kol., 2020) pomocí měření změn membránového potenciálu a dalších metod.
Membrány kvasinek obvykle obsahují ergosterol a žádný cholesterol, který je hlavním sterolem v savčích buňkách. Ergosterol je nezbytný pro regulaci permeability a fluidity membrány, a pro regulaci aktivity membránových transportérů. Díky své nepostradatelné fyziologické roli se ergosterol a jeho biosyntéza staly hlavními cíli pro vývoj antimykotik. Za zvláštních podmínek může savčí cholesterol nahradit ergosterol v jeho klíčové roli, např. některé patogenní kvasinky, jako je Candida glabrata a C. krusei, jsou schopny importovat exogenní cholesterol ze séra hostitele a začlenit jej do svých membrán, aby kompenzovaly nedostatek ergosterolu způsobený podáváním inhibitorů biosyntézy ergosterolu nebo se chránily před polyeny jako je amfotericin B. Pro studium tohoto mechanismu rezistence používáme jako model kvasinky S. cerevisiae, které se v nepřítomnosti kyslíku stávají sterolovými auxotrofy. Kvasinky S. cerevisiae jsou schopny importovat cholesterol a jiné steroly a začleňovat je do plazmatické membrány při anaerobních podmínkách nebo aerobních podmínkách, pokud mají buňky speciální mutaci hem1Δ.
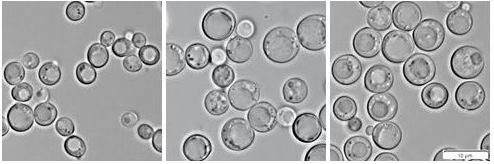
Různá morfologie a velikost buněk s mutací hem1Δ kultivovanýchv přítomnosti ergosterolu (vlevo), cholesterolu (uprostřed) a meziproduktu cholesterolové biosyntézy 7-dehydrocholesterolu (vpravo).
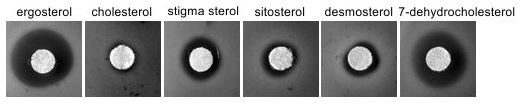
Rezistence buněk hem1∆ akumulujících alternativní steroly k polyenu nystatinu v porovnání s buňkami akumulujícími ergosterol.
Objasňujeme procesy transportu sterolů v kvasinkových buňkách, v nichž je antimykotiky narušena syntéza sterolů. Tato nová zjištění ukazují, jak sterolové složení membrány přispívá k rezistenci kvasinek k antimykotikům.
